L’ÉTUDE CHAMPION*
PRÉVENTION DE L’HÉMORRAGIE AU MOYEN DE LA CARBÉTOCINE (CARBETOCIN HAEMORRHAGE PREVENTION)2
UNE COLLABORATION ENTRE L’OMS, FERRING ET MERCK FOR MOTHERS1
- Ferring Pharmaceuticals et Merck, dans le cadre du projet caritatif MSD for Mothers, ont approché l’Organisation mondiale de la Santé (OMS) afin d’étudier l’utilisation de la carbétocine thermostable2, 3.
- L’étude CHAMPION a comparé l’ocytocine avec une préparation thermostable de carbétocine, et a démontré que la préparation thermostable de carbétocine était non inférieure à l’ocytocine chez les femmes présentant une perte sanguine de ≥500 mL ou avec l’utilisation d’agents utérotoniques supplémentaire; 14,5 % pour la carbétocine par rapport à 14,4 % pour l’ocytocine [risque relatif : 1,02; IC à 95 % : 0,95-1,06]
-
— La proportion de femmes ayant une perte sanguine de ≥ 1 000 ml à 1 heure et jusqu’à 2 heures pour les femmes ayant des saignements persistants après 1 heure était de 1,51 % dans le groupe de la carbétocine et de 1,45 % dans le groupe de l’ocytocine (risque relatif : 1,04; IC à 95 % : 0,87-1,25), avec un intervalle de confiance qui franchit la marge de noninfériorité*.
-
-
* Essai randomisé à double insu de non-infériorité. 23 sites d’étude, 10 pays; n = 29 645 femmes. L’injection intramusculaire de carbétocine thermostable (1 dose de 100 μg) a été comparée à l’administration d’ocytocine (1 dose de 10 UI) immédiatement après l’accouchement vaginal. Critères de jugement principaux : La proportion de femmes ayant une perte sanguine de > 500 ml ou l’utilisation d’agents utérotoniques supplémentaires; et la proportion de femmes ayant une perte sanguine de ≥ 1 000 ml, et jusqu’à 2 heures pour les femmes ayant des saignements persistants après 1 heure. Les marges de non-infériorité pour le risque relatif de ces critères étaient de 1,16 et de 1,23, respectivement.
MODE D’ACTION ET PHARMACOLOGIE CLINIQUE*
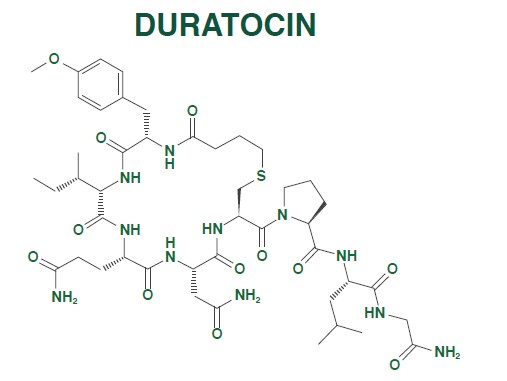
STRUCTURE DE DURATOCIN1
- DURATOCIN est un analogue de l’ocytocine*
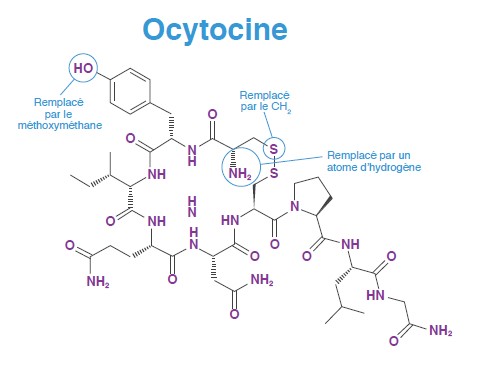
LA CARBÉTOCINE A ÉTÉ CRÉÉE EN APPORTANT PLUSIEURS MODIFICATIONS À LA STRUCTURE DE L’OCYTOCINE4
ACTION PHARMACOLOGIQUE DE LA CARBÉTOCINE1*
- DURATOCIN se lie de façon sélective aux récepteurs de l’ocytocine sur le tissu musculaire lisse de l’utérus.
- La liaison entraîne des contractions rythmiques de l’utérus, augmente la fréquence des contractions existantes et améliore le tonus utérin.
DÉLAI D’ACTION1*
- Une contraction utérine ferme est obtenue dans les 2 minutes suivant l’administration par voie intraveineuse ou intramusculaire.
DURÉE D’ACTION1*
- La durée d’action d’une dose intraveineuse unique de carbétocine sur l’activité utérine est d’environ 1 heure.
DEMI-VIE D’ÉLIMINATION1*
- Selon l’étude de sujets de sexe féminin en bonne santé ayant reçu des doses de 400 à 800 mcg.
- La dose de DURATOCIN recommandée est de 100 mcg.
- DURATOCIN montre une élimination biphasique après l’administration intraveineuse (IV) avec une pharmacocinétique linéaire dans la plage de doses de 400 à 800 mcg.
- La demi-vie est de 33 minutes après l’administration IV.
- La demi-vie est de 55 minutes après l’administration IM; les pics de concentration sont atteints après 30 minutes.
-
* La signification clinique est inconnue.
SURVOL DU PROFIL D’INNOCUITÉ1
ACCOUCHEMENT VAGINAL* :
- Dans un essai comparatif clinique randomisé de grande envergure mené à double insu avec traitement de référence, 14 754 femmes ont reçu de la carbétocine (IM) et 14 743 autres, de l’ocytocine (IM). La carbétocine (100 mcg) et l’ocytocine (10 UI) ont un profil d’innocuité similaire pour la prévention de l’hémorragie post-partum (HPP) après l’accouchement vaginal. Le tableau 1 ci-dessous résume les réactions indésirables liées au traitement1
- Les réactions indésirables les plus fréquentes dans le groupe de la carbétocine (≥ 0,2 % et < 1 %) étaient l’anémie, la douleur abdominale, les vomissements, la pyrexie, l’enflure après l’intervention et l’hémorragie post-partum.
TABLEAU 1 : RÉSUME DES RÉACTIONS INDÉSIRABLES LIÉES AU TRAITEMENT (RILT) DANS L’ÉTUDE A65870
| CARBÉTOCINE (N = 14 754) |
OCYTOCINE (N = 14 743) |
TOTAL (N = 29 497) |
||||
|---|---|---|---|---|---|---|
| n | % | n | % | n | % | |
| Participantes ayant présenté au moins une RILT |
595 | 4,03 | 578 | 3,92 | 595 | 3.98 |
CÉSARIENNE :
- Lors des essais cliniques, les réactions indésirables observées avec la carbétocine étaient de même type et de même fréquence qu’avec l’ocytocine et le placebo pour l’administration après une césarienne sous péridurale ou rachianesthésie.
- Dans les essais cliniques portant sur la césarienne planifiée, les effets indésirables très fréquemment observés (> 1/10) sont les suivants : maux de tête, tremblements, hypotension, bouffées vasomotrices, nausées, douleur abdominale, vomissements, prurit, sensation de chaleur.
-
* Un essai randomisé comparatif avec traitement de référence a été mené à double insu et en parallèle auprès de femmes enceintes en bonne santé devant accoucher par voie vaginale pour établir l’efficacité de la carbétocine (IM) dans la prévention de l’hémorragie post-partum après l’accouchement vaginal. Les patientes ont été affectées au hasard pour recevoir une dose unique par injection IM de 100 mcg de DURATOCIN (n = 14 771) ou de 10 UI d’ocytocine (n = 14 768). Critère de jugement principal : perte sanguine ≥ 500 ml ou utilisation d’agents utérotoniques supplémentaires
EFFICACITÉ DE DURATOCIN EN CAS DE CÉSARIENNE D’URGENCE
DURATOCIN (IV) PAR RAPPORT À L’OCYTOCINE (IV)
DURATOCIN de Ferring (100 mcg IV + 10 ml de soluté lactate de Ringer injecté directement dans la veine sur 2 minutes) a donné des résultats significativement meilleurs par rapport à la césarienne d’urgence avec administration d’ocytocine (20 UI d’ocytocine diluée dans 1 000 ml de soluté lactate de Ringer et administrée par voie intraveineuse à un débit de 125 ml/h).
CHEZ LES FEMMES ENCEINTES DEVANT SUBIR UNE CÉSARIENNE D’URGENCE1‡
- Hémorragie post-partum : 2 % avec DURATOCIN vs 13 % avec l’ocytocine (p = 0,03);
- Perte sanguine estimée : 689 ± 580 mL avec DURATOCIN vs 1 027 ± 659 mL avec l’ocytocine (p = 0,002);
- Transfusion requise : 0 % avec DURATOCIN vs 16 % avec l’ocytocine (p = 0,04)
- Recours à des agents utérotoniques supplémentaires : 2 % avec DURATOCIN vs 71 % avec l’ocytocine (p = 0,002).
-
‡ Essai randomisé comparatif de groupe avec traitement de référence mené à double insu et en parallèle comparant l’efficacité d’une dose de 100 mcg de DURATOCIN (n = 188) avec 5 UI d’ocytocine (n = 189) par injection intraveineuse après une césarienne planifiée ou d’urgence pour prévenir l’hémorragie post-partum (HPP). Critère d’évaluation principal : Incidence de la nécessité d’administrer une dose d’ocytocine supplémentaire1
DURATOCIN EN PRÉVENTION DE L’HÉMORRAGIE POST-PARTUM CHEZ LES FEMMES NULLIPARES ATTEINTES D’OBÉSITÉ
- El-Behery et coll. ont signalé une différence significative quant à la perte sanguine estimée et l’incidence de l’hémorragie du post-partum immédiat (≥ 1 000 ml) dans les deux groupes. (100 mcg de carbétocine par voie IV; 20 UI d’ocytocine en perfusion IV sur 8 heures)5†§
-
— La perte sanguine rapportée dans le groupe de la carbétocine était de 689 ± 580 ml par rapport à 1 027 ± 659 ml dans le groupe de l’ocytocine (p = 0,002). — L’incidence de l’HPP dans le groupe de la carbétocine était de 2/90 ou 2,2 % par rapport à 12/90 ou 13,33 % dans le groupe de l’ocytocine (p = 0,03).
-
- Les taux d’hémoglobine avant l’accouchement et 24 heures après l’accouchement étaient similaires. Des agents utérotoniques supplémentaires ont dû être administrés à 2,22 % des patientes dans le groupe de la carbétocine par rapport à 71,11 % dans le groupe de l’ocytocine (p = 0,002).
- Diminution moyenne du taux d’hémoglobine (g/dl) : 1,74 avec la carbétocine par rapport à 0,94 avec l’ocytocine (p = 0,03).
- Des agents utérotoniques supplémentaires ont dû être administrés à 2,22 % des patientes dans le groupe de la carbétocine par rapport à 71,11 % dans le groupe de l’ocytocine (p = 0,002).
- La contractilité utérine était meilleure dans le groupe de la carbétocine à 2 et 12 heures après l’accouchement que dans le groupe de l’ocytocine (p < 0,05).
-
† Le critère de jugement principal était l’hémorragie du post-partum immédiat majeure définie comme une perte sanguine de ≥ 1 000 ml dans les 24 heures suivant l’accouchement, selon la définition de l’Organisation mondiale de la Santé pour l’HPP. § Essai randomisé comparatif avec traitement de référence mené en parallèle, à double insu et à double placebo portant sur des femmes enceintes nullipares et atteintes d’obésité (IMC > 30) devant subir une césarienne d’urgence. Administration de 100 mcg de DURATOCIN par voie IV (n = 90) ou 20 UI d’ocytocine en perfusion IV sur 8 heures (n = 90). Critère de jugement principal : perte sanguine ≥ 1 000 ml dans les 24 heures après l’accouchement. Diminution moyenne du taux d’hémoglobine (g/dl) : 1,74 avec la carbétocine par rapport à 0,94 avec l’ocytocine1.
PARAMÈTRES PHARMACOCINÉTIQUES D’UNE DOSE DE 100 MCG DE DURATOCIN
PARAMÈTRE : MOYENNE GÉOMÉTRIQUE (CV EN %)
| 100 MCG IV DE CARBÉTOCINE (N = 19) |
100 MCG IM DE CARBÉTOCINE (N = 20) |
|
|---|---|---|
| ASC0-∞ (ng*h/ml) | 2,762 (21,6 %) | 2,147 (18,7 %) |
| ASCt (ng*h/ml) | 2,697 (21,8 %) | 2,022 (20,3 %) |
| Cmax (ng/ml) | 7,232 (17,4 %)a | 1,030 (30,4 %) |
| tmax (heure)b | S.O. | 0,500 (0,250-0,750) |
| t½ (heure) | 0,5480 (25,8 %) | 0,9157 (28,4 %) |
ASC0-∞ = aire sous la courbe de la concentration en fonction du temps zéro extrapolé à l’infini; ASCt = aire sous la courbe de la concentration en fonction du temps écoulé entre le temps zéro et la dernière concentration quantifiable; Cmax = concentration maximale observée; CV = coefficient de variation (en pourcentage); IM = intramusculaire;
IV = intraveineuse; S.O. = sans objet; tmax = temps requis pour atteindre la concentration maximale observée; t½ = demi-vie terminale.
a Concentration mesurée 5 minutes après l’administration de la dose. b Les résultats présentés sont des valeurs médianes (minimum, maximum).
RENSEIGNEMENTS SUR L’INNOCUITÉ
Indications et usage clinique :
DURATOCIN (injection de carbétocine) est indiqué pour la prévention de l’hémorragie post-partum en maîtrisant l’atonie utérine.
Contre-indications :
En raison de l’effet prolongé de DURATOCIN par rapport à l’ocytocine, il n’est pas possible d’arrêter les contractions utérines provoquées par DURATOCIN en cessant simplement d’administrer le médicament.
Par conséquent, DURATOCIN ne doit pas être administré dans les cas suivants :
- Avant l’expulsion ou l’extraction du bébé pour quelque raison que ce soit, même en cas d’un déclenchement artificiel du travail planifié ou médical.
- Chez les patientes ayant des antécédents d’hypersensibilité à l’ocytocine ou à DURATOCIN.
- Chez les patientes ayant des troubles cardiovasculaires graves.
- L’utilisation de DURATOCIN n’est pas recommandée chez les enfants.
Mises en garde et précautions pertinentes :
- DURATOCIN doit seulement être utilisé dans une unité d’obstétrique bien équipée.
- Chez certaines patientes, les contractions pourraient ne pas être adéquates après une dose unique, mais il est déconseillé d’administrer une deuxième dose de DURATOCIN. Il est recommandé de recourir à un traitement plus énergique au moyen d’autres médicaments utérotoniques, tels que l’ocytocine ou l’ergométrine. Il y a lieu d’écarter la présence de fragments placentaires, d’une coagulopathie ou d’un traumatisme du tractus génital en cas de saignements persistants.
- DURATOCIN est conçu pour une administration unique, par voie intramusculaire (IM) ou intraveineuse (IV).
- L’administration de DURATOCIN ne devrait pas produire un effet antidiurétique significatif; aucun effet antidiurétique significatif n’a été démontré à la dose recommandée.
- En raison de l’effet antidiurétique, le risque d’intoxication par l’eau ne peut être exclu.
- Les patientes atteintes d’éclampsie ou de pré-éclampsie doivent faire l’objet d’une surveillance pour détecter tout signe ou symptôme.
- L’utilisation de DURATOCIN n’a pas été étudiée chez des patientes atteintes d’une coagulopathie connue ou qui présentent des signes d’atteinte hépatique, rénale ou endocrinienne.
- DURATOCIN doit être utilisé avec une extrême prudence chez les patientes atteintes d’une maladie cardiovasculaire, en particulier une coronaropathie.
- Aucune étude n’a été menée sur l’utilisation en cas de diabète sucré gestationnel.
- DURATOCIN doit être utilisé avec prudence en cas de migraine et d’épilepsie.
- DURATOCIN doit être utilisé avec prudence en cas d’asthme.
- Chez les femmes qui allaitent, on s’attend à ce que la petite quantité de DURATOCIN transférée dans le lait maternel ou le colostrum après une seule dose de 70 mcg ne présente pas de risque important pour la sécurité. Les données probantes ne sont pas suffisantes pour déterminer si la dose stimule la montée de lait.
- L’administration n’est pas recommandée chez les enfants (< 18 ans) ou les personnes âgées (> 65 ans).
Pour de plus amples renseignements :
Consultez la monographie de produit de DURATOCIN à l’adresse https://www.ferring.ca/media/1257/duratocin-vial-pm-control-no-225949_fr-21feb2020-ver1.pdf pour obtenir des renseignements importants sur les contre-indications, les mises en garde, les précautions, les effets indésirables, les interactions médicamenteuses, la posologie et les conditions d’utilisation clinique. Il est aussi possible d’obtenir la monographie de produit en communiquant avec le service d’information médicale de Ferring par téléphone au 1-866-384-1314.
ADMINISTRATION DE DURATOCIN
- DURATOCIN stable à température ambiante peut être administré en cas d’accouchement vaginal (IM ou IV) ou de césarienne (IV)1.
ADMINISTRATION PAR VOIE IM OU IV EN CAS D’ACCOUCHEMENT VAGINAL1
- Administrer une dose unique de 100 mcg (1 ml) de DURATOCIN par injection intramusculaire ou en bolus lent sur 1 minute, sous surveillance médicale adéquate.
- DURATOCIN doit être administré dès que possible après l’accouchement, de préférence avant l’expulsion du placenta.
- Aucune autre dose de DURATOCIN ne doit être administrée.
ADMINISTRATION PAR VOIE IV EN CAS DE CÉSARIENNE1
- Administrer une dose intraveineuse unique de 100 mcg (1 ml) de DURATOCIN en bolus lent sur 1 minute seulement après l’extraction complète du bébé par césarienne sous péridurale ou rachianesthésie.
- DURATOCIN peut être administré avant ou après l’expulsion du placenta.
- Aucune autre dose de DURATOCIN ne doit être administrée.
DURATOCIN EST MAINTENANT OFFERT SOUS FORME DE FIOLES STABLES À TEMPÉRATURE AMBIANTE
RENSEIGNEMENTS SUR L’INNOCUITÉ
Indications et usage clinique :
DURATOCIN (injection de carbétocine) est indiqué pour la prévention de l’hémorragie post-partum en maîtrisant l’atonie utérine.
Contre-indications :
En raison de l’effet prolongé de DURATOCIN par rapport à l’ocytocine, il n’est pas possible d’arrêter les contractions utérines provoquées par DURATOCIN en cessant simplement d’administrer le médicament.
Par conséquent, DURATOCIN ne doit pas être administré dans les cas suivants :
- Avant l’expulsion ou l’extraction du bébé pour quelque raison que ce soit, même en cas d’un déclenchement artificiel du travail planifié ou médical.
- Chez les patientes ayant des antécédents d’hypersensibilité à l’ocytocine ou à DURATOCIN.
- Chez les patientes ayant des troubles cardiovasculaires graves.
- L’utilisation de DURATOCIN n’est pas recommandée chez les enfants.
Mises en garde et précautions pertinentes :
- DURATOCIN doit seulement être utilisé dans une unité d’obstétrique bien équipée.
- Chez certaines patientes, les contractions pourraient ne pas être adéquates après une dose unique, mais il est déconseillé d’administrer une deuxième dose de DURATOCIN. Il est recommandé de recourir à un traitement plus énergique au moyen d’autres médicaments utérotoniques, tels que l’ocytocine ou l’ergométrine. Il y a lieu d’écarter la présence de fragments placentaires, d’une coagulopathie ou d’un traumatisme du tractus génital en cas de saignements persistants.
- DURATOCIN est conçu pour une administration unique, par voie intramusculaire (IM) ou intraveineuse (IV).
- L’administration de DURATOCIN ne devrait pas produire un effet antidiurétique significatif; aucun effet antidiurétique significatif n’a été démontré à la dose recommandée.
- En raison de l’effet antidiurétique, le risque d’intoxication par l’eau ne peut être exclu.
- Les patientes atteintes d’éclampsie ou de pré-éclampsie doivent faire l’objet d’une surveillance pour détecter tout signe ou symptôme.
- L’utilisation de DURATOCIN n’a pas été étudiée chez des patientes atteintes d’une coagulopathie connue ou qui présentent des signes d’atteinte hépatique, rénale ou endocrinienne.
- DURATOCIN doit être utilisé avec une extrême prudence chez les patientes atteintes d’une maladie cardiovasculaire, en particulier une coronaropathie.
- Aucune étude n’a été menée sur l’utilisation en cas de diabète sucré gestationnel.
- DURATOCIN doit être utilisé avec prudence en cas de migraine et d’épilepsie.
- DURATOCIN doit être utilisé avec prudence en cas d’asthme.
- Chez les femmes qui allaitent, on s’attend à ce que la petite quantité de DURATOCIN transférée dans le lait maternel ou le colostrum après une seule dose de 70 mcg ne présente pas de risque important pour la sécurité. Les données probantes ne sont pas suffisantes pour déterminer si la dose stimule la montée de lait.
- L’administration n’est pas recommandée chez les enfants (< 18 ans) ou les personnes âgées (> 65 ans).
Pour de plus amples renseignements :
Consultez la monographie de produit de DURATOCIN à l’adresse https://www.ferring.ca/media/1257/duratocin-vial-pm-control-no-225949_fr-21feb2020-ver1.pdf pour obtenir des renseignements importants sur les contre-indications, les mises en garde, les précautions, les effets indésirables, les interactions médicamenteuses, la posologie et les conditions d’utilisation clinique. Il est aussi possible d’obtenir la monographie de produit en communiquant avec le service d’information médicale de Ferring par téléphone au 1-866-384-1314.
SURVOL DES CARACTÉRISTIQUES PRINCIPALES DE DURATOCIN
- Administrer une dose unique de 100 mcg en cas d’accouchement vaginal (IM ou IV) ou de césarienne (IV)1.
- En cas d’accouchement vaginal, administrer une dose unique de 100 mcg par voie IM ou IV en bolus lent sur 1 minute.
- Il a été démontré que DURATOCIN réduit le besoin d’administrer des agents utérotoniques supplémentaires chez les femmes enceintes qui présentent un risque accru d’hémorragie post-partum et devant subir une césarienne1.
– Des agents utérotoniques supplémentaires ont dû être administrés chez 2 % des patientes du groupe de la carbétocine comparativement à 71 % dans le groupe de l’ocytocine (p = 0,0002)‡.
-
‡ Essai randomisé comparatif avec traitement de référence mené à double insu et en parallèle comparant l’efficacité d’une dose de 100 mcg de DURATOCIN (n = 188) avec une dose de 5 UI d’ocytocine (n = 189) administrées par voie intraveineuse après une césarienne planifiée ou d’urgence pour prévenir l’hémorragie post-partum (HPP). Critère d’évaluation principal : Incidence de la nécessité d’administrer une dose d’ocytocine supplémentaire1
EFFICACITÉ DÉMONTRÉE À PRÉVENIR L’HÉMORRAGIE POST-PARTUM EN CONTRÔLANT L’ATONIE UTÉRINE1
- Pour les accouchements vaginaux, l’administration de DURATOCIN par voie IM s’est avérée au moins aussi efficace que l’ocytocine par voie IM relativement à la perte sanguine d’au moins 500 ml ou à la nécessité d’administrer des agents utérotoniques supplémentaires1*
- La contractilité utérine s’est révélée supérieure avec DURATOCIN par voie IV qu’avec l’ocytocine à 2 heures et à 12 heures après la césarienne d’urgence (p < 0,05)1*
-
* Essai clinique randomisé contrôlé à double insu. N = 180 femmes enceintes avec un IMC > 30 affectées au hasard dans deux groupes pour recevoir de l’ocytocine (2 ampoules; 20 UI) ou DURATOCIN (100 mcg) par voie IV pendant la césarienne. Critère de jugement principal : hémorragie du postpartum immédiat majeure de ≥ 1 000 mldans les 24 heures suivant l’accouchement. Critères de jugement secondaires :changements du taux d’hémoglobine et de l’hématocrite avant et après l’accouchement; utilisation d’agents utérotoniques supplémentaires; tonus utérin; effets indésirables. Résultats de l’étude : Hémorragie du post-partum immédiat majeure : 2,22 % avec DURATOCIN par rapport à 13,33 % avec l’ocytocine (p = 0,03). Taux d’hémoglobine post-partum : 11,4 ± 1,76 g/dL avec DURATOCIN par rapport à 10,8 ± 1,68 g/dL avec l’ocytocine (p = 0,09). Utérus souple (tonus utérin) : 2,22 % avec DURATOCIN par rapport à 15,55 % avec l’ocytocine (p< 0,05). Besoin d’agents utérotoniques supplémentaires : 2,22 % avec DURATOCIN par rapport à 71,11 % avec l’ocytocine (p< 0,005)
RENSEIGNEMENTS SUR L’INNOCUITÉ
Indications et usage clinique :
DURATOCIN (injection de carbétocine) est indiqué pour la prévention de l’hémorragie post-partum en maîtrisant l’atonie utérine.
Contre-indications :
En raison de l’effet prolongé de DURATOCIN par rapport à l’ocytocine, il n’est pas possible d’arrêter les contractions utérines provoquées par DURATOCIN en cessant simplement d’administrer le médicament.
Par conséquent, DURATOCIN ne doit pas être administré dans les cas suivants :
- Avant l’expulsion ou l’extraction du bébé pour quelque raison que ce soit, même en cas d’un déclenchement artificiel du travail planifié ou médical.
- Chez les patientes ayant des antécédents d’hypersensibilité à l’ocytocine ou à DURATOCIN.
- Chez les patientes ayant des troubles cardiovasculaires graves.
- L’utilisation de DURATOCIN n’est pas recommandée chez les enfants.
Mises en garde et précautions pertinentes :
- DURATOCIN doit seulement être utilisé dans une unité d’obstétrique bien équipée.
- Chez certaines patientes, les contractions pourraient ne pas être adéquates après une dose unique, mais il est déconseillé d’administrer une deuxième dose de DURATOCIN. Il est recommandé de recourir à un traitement plus énergique au moyen d’autres médicaments utérotoniques, tels que l’ocytocine ou l’ergométrine. Il y a lieu d’écarter la présence de fragments placentaires, d’une coagulopathie ou d’un traumatisme du tractus génital en cas de saignements persistants.
- DURATOCIN est conçu pour une administration unique, par voie intramusculaire (IM) ou intraveineuse (IV).
- L’administration de DURATOCIN ne devrait pas produire un effet antidiurétique significatif; aucun effet antidiurétique significatif n’a été démontré à la dose recommandée.
- En raison de l’effet antidiurétique, le risque d’intoxication par l’eau ne peut être exclu.
- Les patientes atteintes d’éclampsie ou de pré-éclampsie doivent faire l’objet d’une surveillance pour détecter tout signe ou symptôme.
- L’utilisation de DURATOCIN n’a pas été étudiée chez des patientes atteintes d’une coagulopathie connue ou qui présentent des signes d’atteinte hépatique, rénale ou endocrinienne.
- DURATOCIN doit être utilisé avec une extrême prudence chez les patientes atteintes d’une maladie cardiovasculaire, en particulier une coronaropathie.
- Aucune étude n’a été menée sur l’utilisation en cas de diabète sucré gestationnel.
- DURATOCIN doit être utilisé avec prudence en cas de migraine et d’épilepsie.
- DURATOCIN doit être utilisé avec prudence en cas d’asthme.
- Chez les femmes qui allaitent, on s’attend à ce que la petite quantité de DURATOCIN transférée dans le lait maternel ou le colostrum après une seule dose de 70 mcg ne présente pas de risque important pour la sécurité. Les données probantes ne sont pas suffisantes pour déterminer si la dose stimule la montée de lait.
- L’administration n’est pas recommandée chez les enfants (< 18 ans) ou les personnes âgées (> 65 ans).
Pour de plus amples renseignements :
Consultez la monographie de produit de DURATOCIN à l’adresse https://www.ferring.ca/media/1257/duratocin-vial-pm-control-no-225949_fr-21feb2020-ver1.pdf pour obtenir des renseignements importants sur les contre-indications, les mises en garde, les précautions, les effets indésirables, les interactions médicamenteuses, la posologie et les conditions d’utilisation clinique. Il est aussi possible d’obtenir la monographie de produit en communiquant avec le service d’information médicale de Ferring par téléphone au 1-866-384-1314.
CENTRE DE RESSOURCES
RENSEIGNEMENTS SUR L’INNOCUITÉ
Indications et usage clinique :
DURATOCIN (injection de carbétocine) est indiqué pour la prévention de l’hémorragie post-partum en maîtrisant l’atonie utérine.
Contre-indications :
En raison de l’effet prolongé de DURATOCIN par rapport à l’ocytocine, il n’est pas possible d’arrêter les contractions utérines provoquées par DURATOCIN en cessant simplement d’administrer le médicament.
Par conséquent, DURATOCIN ne doit pas être administré dans les cas suivants :
- Avant l’expulsion ou l’extraction du bébé pour quelque raison que ce soit, même en cas d’un déclenchement artificiel du travail planifié ou médical.
- Chez les patientes ayant des antécédents d’hypersensibilité à l’ocytocine ou à DURATOCIN.
- Chez les patientes ayant des troubles cardiovasculaires graves.
- L’utilisation de DURATOCIN n’est pas recommandée chez les enfants.
Mises en garde et précautions pertinentes :
- DURATOCIN doit seulement être utilisé dans une unité d’obstétrique bien équipée.
- Chez certaines patientes, les contractions pourraient ne pas être adéquates après une dose unique, mais il est déconseillé d’administrer une deuxième dose de DURATOCIN. Il est recommandé de recourir à un traitement plus énergique au moyen d’autres médicaments utérotoniques, tels que l’ocytocine ou l’ergométrine. Il y a lieu d’écarter la présence de fragments placentaires, d’une coagulopathie ou d’un traumatisme du tractus génital en cas de saignements persistants.
- DURATOCIN est conçu pour une administration unique, par voie intramusculaire (IM) ou intraveineuse (IV).
- L’administration de DURATOCIN ne devrait pas produire un effet antidiurétique significatif; aucun effet antidiurétique significatif n’a été démontré à la dose recommandée.
- En raison de l’effet antidiurétique, le risque d’intoxication par l’eau ne peut être exclu.
- Les patientes atteintes d’éclampsie ou de pré-éclampsie doivent faire l’objet d’une surveillance pour détecter tout signe ou symptôme.
- L’utilisation de DURATOCIN n’a pas été étudiée chez des patientes atteintes d’une coagulopathie connue ou qui présentent des signes d’atteinte hépatique, rénale ou endocrinienne.
- DURATOCIN doit être utilisé avec une extrême prudence chez les patientes atteintes d’une maladie cardiovasculaire, en particulier une coronaropathie.
- Aucune étude n’a été menée sur l’utilisation en cas de diabète sucré gestationnel.
- DURATOCIN doit être utilisé avec prudence en cas de migraine et d’épilepsie.
- DURATOCIN doit être utilisé avec prudence en cas d’asthme.
- Chez les femmes qui allaitent, on s’attend à ce que la petite quantité de DURATOCIN transférée dans le lait maternel ou le colostrum après une seule dose de 70 mcg ne présente pas de risque important pour la sécurité. Les données probantes ne sont pas suffisantes pour déterminer si la dose stimule la montée de lait.
- L’administration n’est pas recommandée chez les enfants (< 18 ans) ou les personnes âgées (> 65 ans).
Pour de plus amples renseignements :
Consultez la monographie de produit de DURATOCIN à l’adresse https://www.ferring.ca/media/1257/duratocin-vial-pm-control-no-225949_fr-21feb2020-ver1.pdf pour obtenir des renseignements importants sur les contre-indications, les mises en garde, les précautions, les effets indésirables, les interactions médicamenteuses, la posologie et les conditions d’utilisation clinique. Il est aussi possible d’obtenir la monographie de produit en communiquant avec le service d’information médicale de Ferring par téléphone au 1-866-384-1314.
Références :
- Monographie de DURATOCIN®. Ferring Inc. 21 février, 2020.
- Widmer M, et coll. « Heat-stable carbetocin versus oxytocin to prevent hemorrhage after vaginal birth ». N Engl J Med 2018;379(8):743e52. (CHAMPION Study) https://www.nejm.org/doi/full/10.1056/NEJMoa1805489
- « WHO recommendations: Uterotonics for the prevention of postpartum haemorrhage. Web annex 2: Carbetocin versus placebo or no treatment: Evidence to Decision framework ». Geneva: World Health Organization; 2018 (WHO/RHR/18.29). Licence: CC BY-NC-SA 3.0 IGO.
- Cordovani D, et coll. « Carbetocin at elective Caesarean delivery: a randomized controlled trial to determine the effective dose ». Can J Anesth/J Can Anesth. 2012:59:751–757. DOI 10.1007/s12630-012-9728-2
- El Behery, et coll. « Carbetocin versus oxytocin for prevention of postpartum haemorrhage in obese nulliparous women undergoing emergency caesarean delivery ». J Matern Fetal Neonatal Med 2016;29(8):1257-60., DOI:10.3109/14767058.2015.1043882
® Marque déposée de Ferring B.V.
COURRIEL: CA0-MEDICALINFORMATI@FERRING.COM .TÉLÉPHONE: 1-866-384-1314
© 2021 FERRING INC.
Tous droits réservés.
Cervidil® et Duratocin® sont des marques déposées de Ferring B.V.


 BALADOS
BALADOS